En este lugar te compartimos el material educativo de Estructura Atómica para Cuarto Grado de Secundaria o estudiantes de 15 años de edad, que podrás obtener GRATIS en formato PDF. Este contenido pertenece al curso de QUÍMICA.
Muestra del Material Educativo
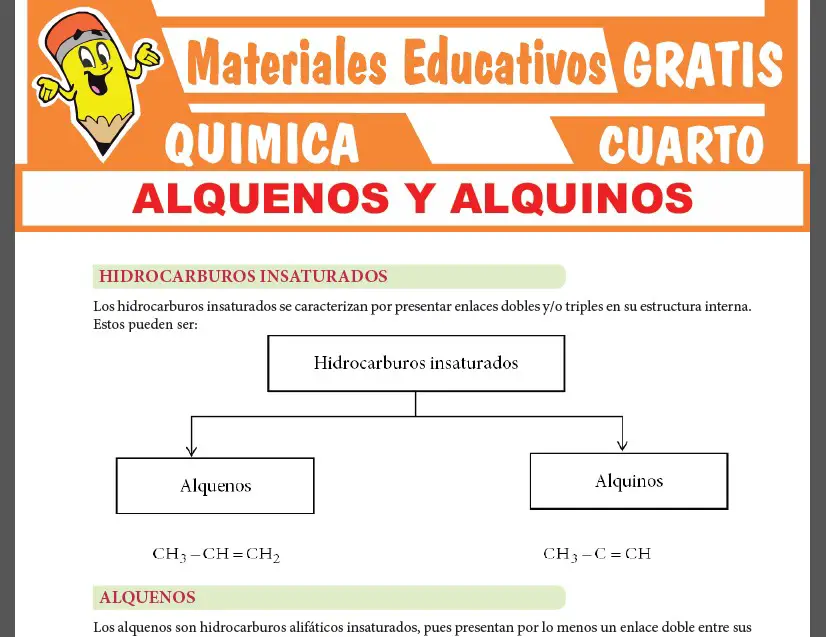
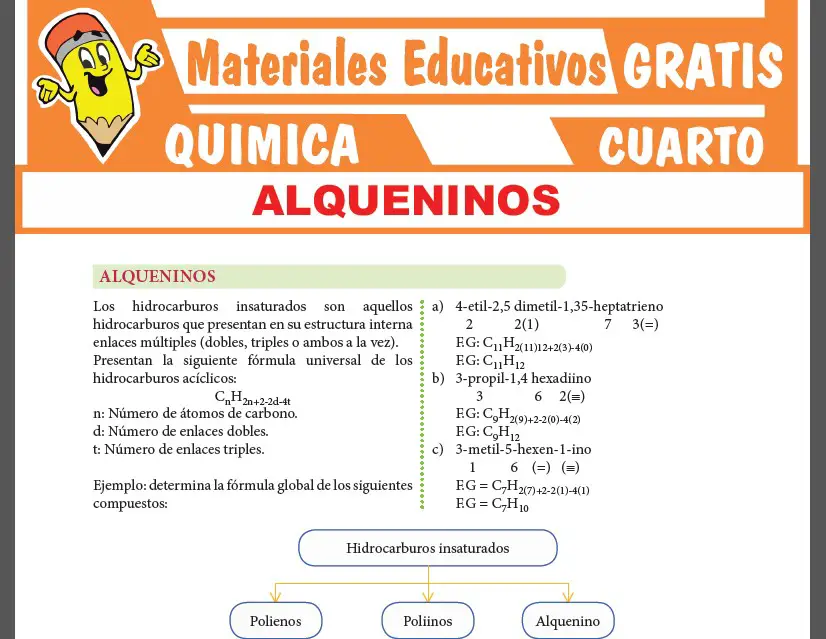
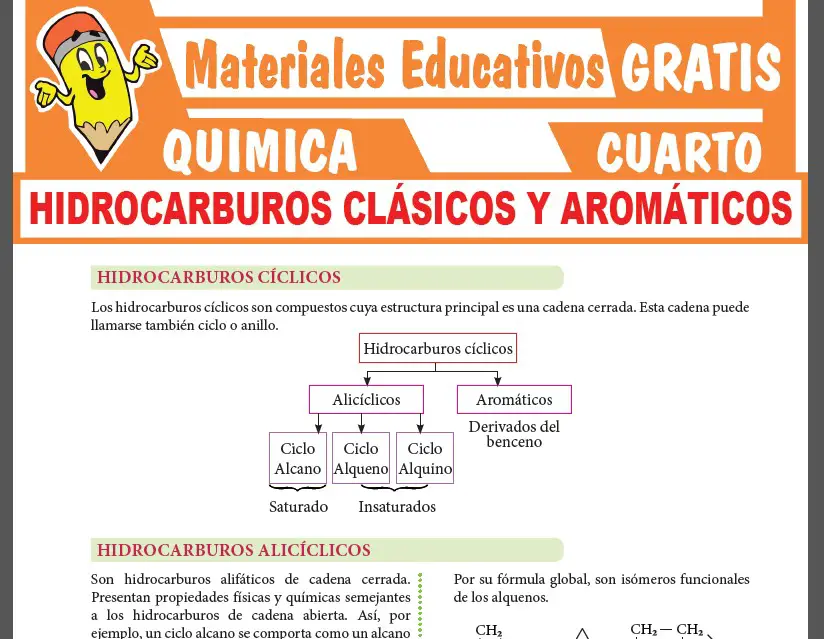
En esta parte te presentaremos una MUESTRA de la 1era PÁGINA de la ficha de Estructura Atómica que podrás descargar GRATIS.
 Este material educativo de Estructura Atómica lo podrás adquirir de forma sencilla y gratuita a continuación:
Este material educativo de Estructura Atómica lo podrás adquirir de forma sencilla y gratuita a continuación:
Descarga GRATIS este Material Educativo
En esta parte te presentaremos los enlaces de descarga para que obtengas esta maravillosa ficha de Estructura Atómica.
Opción A – PDF | Opción B – PDF
¿Qué Contiene este Ficha Educativa que te Compartimos?
Esta ficha de Modelos Atómico que podrás adquirir contiene estos temas:
- Historia del Átomo.
- Modelos Atómicos.
- Actividades para desarrollar.
Ahora desarrollaremos algunos de estos conceptos teóricos:
Historia del Átomo
El concepto del átomo fue planteado por los filósofos griegos Leucipo y Demócrito (400 a. C.) quienes planteaban que todos los cosas están constituidas por partículas muy pequeñas, indivisibles e indestructibles. La palabra átomo etimológicamente significa sin división. Esta teoría nunca fue aceptada por Aristóteles, el filósofo más importante de su época, por lo cual fue abandonada durante 2000 años.
Modelos Atómicos
Estos son los siguientes:
Teoría atómica de Dalton (1808)
John Dalton retoma el concepto de átomo y empieza a estudiarlo de una forma científica y no filosófica. Su modelo se basa en 4 postulados, enunciados en su trabajo científico.
Modelo atómico de Thomson (1897)
Joseph Thomson sustenta su modelo «budin de pasas, basado en un átomo de forma esférica y con masa compacta y carga positiva, distribuida homogéneamente.
Modelo de Rutherford (1911)
Ernest Rutherford plantea su modelo atómico conocido como «sistema planetario en miniatura». Dio a conocer una imagen distinta del átomo hasta ese momento pues afirma que el átomo posee una parte central muy pequeña llamada núcleo, donde se encuentran los protones, los electrones que giran a su alrededor en trayectorias circulares y concéntricas, contrarrestando con este movimiento la fuerza de atracción de la carga positiva del núcleo.
Modelo atómico de Bohr (1913)
Niels Bohr propuso el modelo del átomo para explicar cómo los electrones giran alrededor del núcleo en orbitas circulares llamadas 2 niveles estacionarias de energía.
Modelo atómico de Bohr-Sommerfield (1913)
Arnold Somemmerfield formuló la existencia de los subniveles de energía, sostuvo que los electrones, aparte de seguir órbitas circulares, tambien seguían órbitas elípticas, con ello explica el efecto Zeeman.
Definiciones Básicas
Estas son las siguientes:
Número atómico (Z)
Llamado carga nuclear, determina la cantidad de protones que tiene un átomo neutro.
Número de masa (A)
Llamado número másico, es la suma de los protones y los neutrones de un átomo (nucleones).
Representación de núclidos
Se representan de la siguiente manera:
Iones
Llamadas especies iónicas son aquellos átomos o conjuntos de átomos compuestos de átomos que presentan cargas eléctricas, como consecuencia pueden ganar o perder uno o más electrones.
Clasificación de Núclidos
En la clasificación tenemos:
Isótopos
Átomos de un mismo elemento químico, igual Z.
Isóbaros
Átomos de diferentes elementos con igual número de masa.
Isótonos
Átomos de diferentes elementos con igual número de electrones (n°).
Actividades de la Ficha de Estructura Atómica
En este material educativo también hallaras muchas actividades de Modelos Atómico, donde los estudiantes de cuarto grado podrán trabajar de forma individual o con la ayuda del docente.
Ahora te presentaremos algunas de estas actividades:
- El número de masa de un átomo es 56 y neutrones, 26. Determina su número atómico.
- Si el número de masa de un átomo es 63, y el número de neutrones es de 5 unidades más que el número de electrones, calcula el número de protones.
- Si cierto átomo tiene número masico 48, y sus protones y neutrones están en la relación de 5 a 7, calcula su carga nuclear.
- Un catión posee un número de masa igual a 45 y tiene 18 electrones, determina el número total de las partículas elementales que posee.
- Se tienen tres hilidos de un elemento, y uno de sus neutrones 21. Calcula la carga nuclear del isótopo más pesado si se conoce que la suma de los nucleones de dichos átomos es 57.
- La suma de los números de masa de 2 isótopos es 84 y la suma de sus neutrones, 44. Calcula el número atómico del isótopo.
Para un aprendizaje optimo, recomendamos que los estudiantes desarrollen el 100% de actividades de Modelos Atómico que están propuestas en el material educativo que te compartimos.
Con tu ayuda podemos ayudar a más docentes y estudiantes, comparte nuestra página web “materialeseducativos.org” con todos tus amigos y colegas.
Más Fichas de Química para Cuarto de Secundaria
En nuestra pagina web también contamos con otras 28 fichas de Química elaboradas para estudiantes que cursan el cuarto de secundaria, aquí te compartimos el enlace que te llevara a estos materiales educativos:
▷ ▷ 28 Fichas de Química para Cuarto Grado ◁ ◁
Si necesitas mas materiales educativos de Química para estudiantes de este mismo grado, ahora te dejaremos otro enlace donde encontraras otros materiales educativos gratuitos:
Otras Fichas de Química de 4to Grado
¿Que te pareció este material educativo de química para cuarto grado?, déjanos tu comentario en la parte de abajo.