Aquí podrás descargar GRATIS la ficha de Termodinámica para Quinto Grado de Secundaria o estudiantes de 16 años. Este tema pertenece al curso de FÍSICA y lo podrás obtener de forma GRATUITA en PDF.
Muestra del Material Educativo
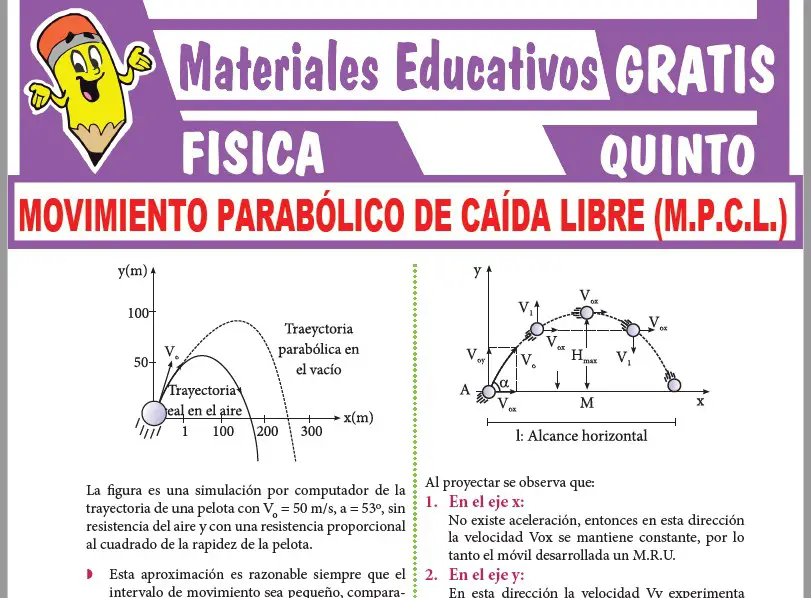
Ahora podrás observar una MUESTRA de la 1era PÁGINA de la ficha de Termodinámica.
 Deseamos que este material educativo de Termodinámica contribuya a la enseñanza y el aprendizaje de este importante tema.
Deseamos que este material educativo de Termodinámica contribuya a la enseñanza y el aprendizaje de este importante tema.
Descarga GRATIS este Material Educativo
En esta parte te dejaremos los enlaces para que puedas descargar este maravilloso material educativo de Termodinámica, elije la opción de tu preferencia:
Opción A – PDF | Opción B – PDF
¿Qué Contiene este Material Educativo que te Ofrecemos?
Esta ficha de Termodinámica contiene contenidos muy importantes, así como:
- Termodinámica
- Actividades para desarrollar.
Ahora desarrollaremos algunos contenidos:
¿Qué estudia la termodinámica?
El intercambio de energía entre sistemas que interactúan térmicamente. En nuestro caso, un sistema sería un gas ideal, otro sistema seria el recipiente que lo contiene, y otros sistemas serían las sustancias que rodean al gas ideal.
¿Los gases ideales tienen energía potencial?
No, porque a nivel molecular, la separación relativa entre las moléculas es muy grande, lo que significa que las interacciones entre ellas son despreciables. Como las moléculas están en constante movimiento, significa que la energía asociada a un gas ideal es cinética, luego:
Si la temperatura de un gas ideal se incrementa, sus moléculas presentan mayor rapidez (V) y, por lo tanto, mayor energía cinética, lo que significa mayo energía interna.
Conceptos preliminares
Estos son los conceptos preliminares:
Sistema termodinámico
Porción de materia que separemos imaginariamente del medio externo a ella y la cual interacciona con su medio ambiente y como consecuencia se da una transferencia de calor.
Sustancia de trabajo
Sustancia empleada como medio de transporte del calor, así como de intermediario en la transformación de calor en trabajo. Usualmente es un gas.
Energía interna (U)
Es aquella energía de un cuerpo que está relacionada con el movimiento térmico de las moléculas que lo forman.
Si no hay cambio de fase, la energía interna es una función de la temperatura absoluta, por lo que el cambio de energía interna solo depende de la temperatura del estado final y la del estado inicial, pero no de la forma como se ha pasado de estado inicial al final.
Proceso termodinámico
Es la sucesión de estados por los cuales se hace pasar un sistema, con la finalidad de transformar calor en trabajo.
El estado de un sistema está determinado por el conjunto de propiedades que posee en un momento dado. Estas propiedades se determinan por ciertas magnitudes, que determinan el comportamiento del sistema, denominadas ≪variables de estado≫.
Ciclo termodinámico
Es una sucesión de procesos, la cual permite evolucionar a un sistema de estado inicial (I) hacia un estado final (F) y volver al inicial, de manera que, durante la realización del ciclo, parte del calor suministrado se convierte en trabajo.
Primera ley de la termodinámica
En todo proceso termodinámico se cumple que la cantidad de calor que se entrega o sustrae a un sistema es igual al trabajo realizado por o sobre el sistema más el cambio correspondiente de energía interna (DU).
Calores específicos de los gases
El calor necesario para elevar la temperatura de un gas depende de cómo se halle confinado. Por ejemplo, si el volumen se mantiene constante, el calor recibido por el gas se convierte totalmente en energía interna, elevando por lo tanto la temperatura.
Trabajo realizado por un gas ideal
Cuando un gas confinado en un recipiente experimenta un proceso de expansión o comprensión desarrolla o consume respectivamente un trabajo el cual depende de la forma como varié la presión y volumen del gas, es decir del proceso realizado.
Observaciones
- Como el cambio de energía interna solo depende del estado final e inicial, siempre se puede relacionar con el cambio de energía interna en un proceso isocora entre las mismas temperaturas:
- La isoterma (en el plano P-V) es una curva simétrica respecto a la bisectriz del primer cuadrante.
- La adiabática es una curva más inclinada que la isoterma, es decir, su pendiente varía más rápidamente.
Máquinas térmicas y la segunda ley de la termodinámica
¿Qué es una maquina térmica?
Es un dispositivo que convierte energía térmica en otras formas útiles de energía, como las energías eléctrica y mecánica.
Esta diseñada con la finalidad de trasformar calor en trabajo, para lo cual la maquina sigue un ciclo termodinámico.
¿Cuál es la función de una maquina térmica?
Que una sustancia de trabajo recorra un proceso cíclico durante el cual ocurre lo siguiente:
- Se absorbe calor de una fuente a alta temperatura.
- La máquina realiza un trabajo, y
- Libera calor a una fuente de temperatura más baja.
Eficiencia térmica (n)
La eficiencia de una maquina térmica (E) se obtiene mediante la relación entre el trabajo realizado y la energía recibida del foco caliente.
Conclusiones de la segunda ley de la termodinámica
- Una maquina térmica no puede tener un rendimiento del 100%. (Kelvin – Planck).
- Es imposible para cualquier proceso tener como único resultado la transferencia de calor desde un cuerpo frio a uno caliente.
Actividades de la Ficha de Termodinámica
En este material educativo también hallaras muchos ejercicios de Termodinámica elaborados de forma especial para los estudiantes de quinto grado.
Ahora te presentaremos algunos de estos ejercicios:
- En cierto proceso químico, un técnico de laboratorio suministra 320 J de calor a un sistema. Si se observa que la energía interna del sistema aumenta en 90 J, ¿cuál es el trabajo realizado por el sistema?
- Un gas encerrado recibe 1200 calorías y su energía interna aumenta 320 J. ¿Qué trabajo realiza el gas? (1 J = 0,24 cal)
- A un gas perfecto se le suministra 200 J de calor isotérmicamente. Halla el trabajo que desarrolla el gas.
- Un sistema termodinámico evoluciona desde un estado (1), P1 = 20 KN/m2; V1 = 3 m3, hasta un estado (2), V2 = 10 m3, isobáricamente. Si recibe una cantidad de calor Q = 100 KJ, halla el cambio de energía interna del sistema.
- Un sistema termodinámico evoluciona desde un estado (1), P1 = 10 KN/m2; V1 = 2 m3, hasta un estado (2), V2 = 8 m3, isobáricamente. Si recibe una cantidad de calor Q = 100 KJ, halla el cambio de energía interna del sistema.
- Un gas, en un cilindro, se mantiene a presión constante de 2,60 × 105 Pa mientras se enfría y se comprime de 1,801 m3 a 1,50 m3. La energía interna del gas disminuye 1,40 × 105 Halla el calor que entra o sale del gas.
Recomendamos que los estudiantes resuelvan todos los ejercicios planteados en esta ficha educativa que te brindamos, esto aportara al aprendizaje de tema importante: Termodinámica.
Recuerda que el recurso educativo que te compartimos en este artículo fue preparado de forma especial para los estudiantes de quinto de secundaria, también contamos con material educativo de los demás grados.
Más Fichas de Física para Quinto de Secundaria
Te comentamos que en este sitio web encontraras mas fichas educativas de física para estudiantes de Quinto de Secundaria, si deseas saber los temas que poseemos, aquí te dejamos el enlace para que lo revises:
▷ ▷ 28 Fichas de Física para Quinto Grado ◁ ◁
Si quieres conocer otra pagina web que también ofrece fichas educativas gratuitas de física de este mismo grado, a continuación te compartiremos el siguiente enlace:
Otras Fichas de Física para 5to Grado
«¿Que opinas acerca de este material educativo de Física para Quinto grado?, puedes dejarnos tu comentario en la parte inferior